
診察時間
午前9:00-12:00
午後15:00-18:00
手術時間12:00-15:00
水曜・日曜午後休診

クッシング🌸ステロイドがたくさん出る病気
-
ステロイドが過剰に分泌される病気です
ステロイドホルモン(別名コルチゾール)は
ストレスに対して対抗したり、
イオンバランスの調整や、
筋肉量の調整に関わっています。
多すぎるとあらゆる悪影響が出てきてしまい、
中には生命にかかわるものもあるので、
注意が必要です。 -
-
-
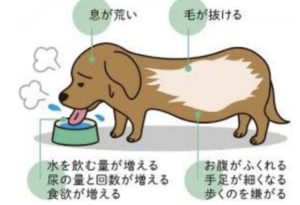
症状
筋肉がうすくなって
脂肪が溜まり、
腹囲膨満(太ってきたり、ポテッ腹に)
呼吸筋がうすくなる
ハァハァとパンティングしたり、
多飲多尿(PUPD、水をたくさん飲み、尿をたくさんする)
血栓傾向になり、
重要な血管に血栓が詰まる事で臓器が機能しなくなります。
肺に血栓が飛び、呼吸困難に陥る事があります。
糖尿病
ステロイドホルモンは血糖値を上げるので10%の子で発症します。
-
-
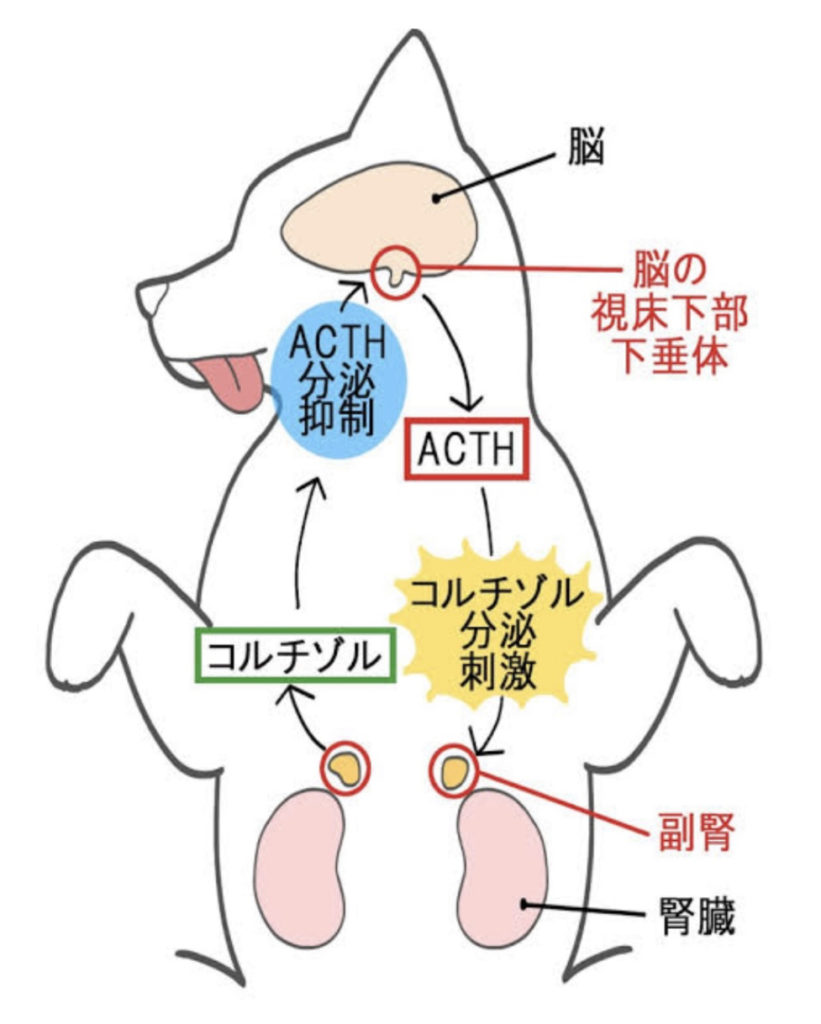
脳の腫瘍が原因
脳下垂体が腫瘍化する(PDH)事で
副腎を刺激するホルモン(ACTH)が多く分泌され、
副腎から多くのステロイドが
分泌されてしまいます。
クッシングの80%はPDH性です。
脳の腫瘍を摘出するのは大きなリスクがあるので、
ステロイドホルモンを遮断する投薬治療を行います。
トリロスタン(商品名;アドレスタン)
原因の治療を行なっているわけではないので、
てんかんや失明などの症状には
引き続き注意が必要です。
クッシングの残り20%は
副腎が腫瘍化するAT型です。
摘出が治療法になります。
-
-
診断
ALPの上昇(90%)
ACTH製剤(コートロシン)を皮下注射して
1時間後のコルチゾール(ステロイド)が
25以上の場合は確定します。
-
-
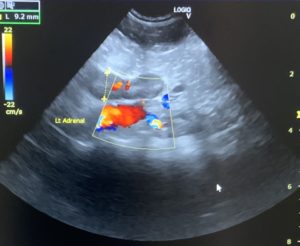
エコー検査
下垂体腫瘍では
ACTHの分泌過剰で副腎が反応して、
両副腎が大きくなります。
副腎腫瘍では
片方の副腎だけが大きくなります。
-
-
投薬中の注意事項
効きすぎてアジソンになっていないか、
お薬が足りているかを症状と血液検査で判断しています。
治療に反応があると体重が減って、
飲水量が減ってきます。
お薬が効きすぎるとアジソン病状態になり、
ストレスによる虚脱
失神やふらつき
脱水
嘔吐、下痢などの消化器症状を
引き起こすため、
投薬初期2週間は注意が必要です。
-
-
継続の診察
ACTH刺激試験を行い、投薬コントロールを見ています。
循環や脱水のチェックとして、
心雑音の有無
ふらつきや吐き気がないか
腎臓、肝臓、電解質バランスの確認をしています。
血液検査は12時間の絶食でご来院をお願いしています。
A disease in which steroids are overproduced
The steroid hormone (also known as cortisol)
to cope with stress,
adjustment of ion balance,
Involved in regulating muscle mass.
If it is too much, all sorts of bad effects will come out,
Some of them are life-threatening,
Caution is required.
symptoms
my muscles are getting weaker
Accumulated fat,
Abdominal bloating
weakened respiratory muscles
Punting with a haha,
Polydipsia and polyuria (PUPD, drinking a lot of water and urinating a lot)
become thrombotic,
Blood clots clog important blood vessels and prevent organs from functioning.
Blood clots can travel to the lungs and cause breathing difficulties.
Diabetes
Since steroid hormones raise blood sugar levels, 10% of children develop the disease.
caused by a brain tumor
By pituitary gland tumor (PDH)
A large amount of hormone (ACTH) that stimulates the adrenal glands is secreted,
Many steroids are released from the adrenal glands
will be secreted.
80% of Cushings are PDH.
The risk of having a brain tumor removed is high.
Administer medication to block steroid hormones.
Trilostane (trade name: Addresstan)
Since we are not treating the cause,
For conditions such as epilepsy and blindness
Continued caution is required.
The remaining 20% of Cushing is
It is an AT type in which the adrenal glands become tumors.
Excision is the cure.
diagnose
Increased ALP (90%)
Subcutaneous injection of ACTH preparation (Cortrocin)
Cortisol (steroid) after 1 hour
25 or more confirms.
echo examination
in pituitary tumors
Excessive secretion of ACTH causes the adrenal glands to react,
Both adrenal glands are enlarged.
in adrenal tumors
Only one adrenal gland is enlarged.
Precautions during administration
Is it too effective to become Addison’s?
Your symptoms and blood tests determine if you are taking enough medicine.
Responsive to treatment, weight loss,
You will drink less water.
Addison’s disease occurs when the drug is too effective.
collapse due to stress
Fainting or light-headedness
dehydration
Gastrointestinal symptoms such as vomiting and diarrhea
to cause
Care should be taken during the first 2 weeks of administration.
follow-up examination
Perform ACTH stimulation tests and look at medication controls.
As a check of circulation and dehydration,
Presence of heart murmur
Do you have lightheadedness or nausea?
Checking kidney, liver and electrolyte balance.
You will be asked to come in for a blood test after fasting for 12 hours.
스테로이드가 과도하게 분비되는 질병입니다.
스테로이드 호르몬 (일명 코르티솔)은
스트레스에 대항하거나,
이온 밸런스 조정 및
근육량 조정에 관여합니다.
너무 많으면 모든 악영향이 나오고,
일부는 생명과 관련된 것도 있으므로,
주의가 필요합니다.
증상
근육이 으르렁거리고
지방이 쌓이고,
배꼽 팽만 (뚱뚱해지거나 감자 배에)
호흡근이 좋다
허하와 펀팅하거나,
다음 다변 (PUPD, 물을 많이 마시고 소변을 많이한다)
혈전 경향이되어,
중요한 혈관에 혈전이 막히면 장기가 작동하지 않습니다.
폐에 혈전이 날아 호흡 곤란에 빠지는 일이 있습니다.
당뇨병
스테로이드 호르몬은 혈당치를 올리므로 10%의 아이로 발병합니다.
뇌의 종양으로 인해
뇌하수체가 종양화 (PDH)
부신을 자극하는 호르몬 (ACTH)이 많이 분비되어
부신에서 많은 스테로이드가
분비되어 버립니다.
쿠싱의 80%는 PDH성입니다.
뇌의 종양을 적출하는 것은 큰 위험이 있기 때문에,
스테로이드 호르몬을 차단하는 투약 치료를 실시합니다.
트리로스탄(상품명;주소탄)
원인의 치료를 실시하고 있는 것은 아니기 때문에,
간질이나 실명 등의 증상에는
계속주의가 필요합니다.
쿠싱의 나머지 20%는
부신이 종양화하는 AT형입니다.
적출이 치료법이 됩니다.
진단
ALP 상승(90%)
ACTH 제제 (코트로신)를 피하 주사하여
1 시간 후 코르티솔 (스테로이드)
25 이상인 경우는 확정합니다.
에코 검사
뇌하수체 종양에서
ACTH의 분비 과잉으로 부신이 반응하여,
두 부신이 커집니다.
부신 종양에서
한쪽 부신만이 커집니다.
투약 중 주의사항
너무 효과적이고 애디슨이 아니거나,
약이 부족한지 증상과 혈액 검사로 판단하고 있습니다.
치료에 반응이 있으면 체중이 줄어들고,
식수량이 줄어듭니다.
약이 너무 효과가 있으면 아디슨 병 상태가되고,
스트레스로 인한 허탈
실신과 흔들림
탈수
구토, 설사 등 소화기 증상
일으키기 위해,
투약 초기 2주일에는 주의가 필요합니다.
지속적인 진찰
ACTH 자극 시험을 실시하고 투약 컨트롤을보고 있습니다.
순환이나 탈수의 체크로서,
심잡음의 유무
흔들림이나 메스꺼움이 없습니까?
신장, 간, 전해질 밸런스를 확인하고 있습니다.
혈액 검사는 12시간의 단식으로 내원을 부탁하고 있습니다.
类固醇分泌过多的疾病
类固醇激素(也称为皮质醇)
为了应对压力,
调节离子平衡,
参与调节肌肉质量。
如果太多了,就会出现各种不好的影响,
有的甚至危及生命,
需要谨慎。
症状
我的肌肉越来越弱
脂肪堆积,
腹胀
呼吸肌减弱
打哈哈,
烦渴多尿(PUPD,多喝水,多排尿)
成为血栓,
血凝块会阻塞重要的血管并阻止器官运作。
血块会移动到肺部并导致呼吸困难。
糖尿病
由于类固醇激素会提高血糖水平,因此 10% 的儿童会患上这种疾病。
由脑瘤引起
垂体瘤(PDH)
分泌大量刺激肾上腺的激素(ACTH),
许多类固醇从肾上腺释放
会被分泌。
80% 的库欣是 PDH。
切除脑瘤的风险很高。
服用药物来阻断类固醇激素。
Trilostane(商品名:Addresstan)
由于我们没有治疗病因,
对于癫痫和失明等疾病
需要继续保持谨慎。
库欣剩下的20%是
它是肾上腺变成肿瘤的AT型。
切除是治疗方法。
诊断
碱性磷酸酶增加 (90%)
皮下注射促肾上腺皮质激素制剂(Cortrocin)
1 小时后皮质醇(类固醇)
25 个或更多确认。
回声检查
垂体瘤
ACTH分泌过多引起肾上腺反应,
两个肾上腺都肿大。
在肾上腺肿瘤
只有一个肾上腺肿大。
给药期间的注意事项
成为艾迪生太有效了吗?
您的症状和验血决定了您是否服用了足够的药物。
对治疗有反应,体重减轻,
你会喝更少的水。
当药物过于有效时,就会发生艾迪生病。
因压力而崩溃
昏厥或头晕目眩
脱水
呕吐、腹泻等胃肠道症状
导致
在给药的前 2 周内应小心。
后续检查
执行 ACTH 刺激测试并查看药物控制。
作为循环和脱水的检查,
存在心脏杂音
你有头晕或恶心吗?
检查肾脏、肝脏和电解质平衡。
您将被要求在禁食 12 小时后进行血液检查。
